1. धातु किसे कहते हैं ?
उत्तर⇒ आवर्त सारणी के बायीं तरफ तथा मध्य में रखे जाने वाले तत्त्व धातु कहलाते हैं, जिनमें धात्विक चमक होती है । वे प्रायः तन्य, आघातवर्ध्य, विद्युत् और ऊष्मा की सुचालक, दृढ़ और अधिक घनत्व वाली होती हैं। इनके ऑक्साइड क्षारीय प्रकृति के होते हैं । लोहा, सोना, चाँदी, ताँबा, प्लैटिनम आदि धातुओं के उदाहरण हैं ।
2. धातुओं के दो रासायनिक गणों को लिखें।
उत्तर⇒(i) धातुओं के ऑक्साइड क्षारीय होते हैं।
(ii) अम्लों से अभिक्रिया कर हाइड्रोजन गैस विस्थापित करते हैं।
2Na +2HCL→ 2NaCl + H 2
3. अधातु के दो गुणधर्मों को लिखें।
उत्तर⇒ (i) अधिकतर अधातुएँ गैसीय अवस्था में पाये जाते हैं।
(ii) अधातुएँ सोनोरस ध्वनि उत्पन्न नहीं करते हैं।
| Also Read : class 10th science objective |
4. कौन-सी धातुएँ आसानी से संक्षारित नहीं होती हैं ?
उत्तर⇒ सोना और चाँदी ऐसी धातुएँ हैं जो अभिक्रियाशीलता श्रेणी में सबसे नीचे आती हैं। ये धातुएँ काफी कम अभिक्रियाशील हैं। ऐसी धातुएँ आसानी से संक्षारित नहीं होती हैं।
5. धातुओं का परिष्करण से क्या तात्पर्य है ?
उत्तर⇒ अपचयन प्रक्रम से प्राप्त धातुएँ शुद्ध नहीं होती हैं। इनमें अपद्रव्य होती हैं। शुद्ध धातु की प्राप्ति इन अपद्रव्यों को धातु से हटाकर किया जाता है। अत: अशुद्ध धातुओं से अपद्रव्यों को हटाना धातुओं का परिष्करण कहा जाता है।
6. ऐसा धातु का उदाहरण दीजिए जो-
(i) कमरे के ताप पर द्रव होता है।
(ii) चाकू से आसानी से काटा जा सकता है।
(iii) ऊष्मा का सबसे अच्छा चालक हाता है।
(iv) ऊष्मा का कुचालक होता है।
उत्तर⇒ (i) पारा (ii) सोडियम तथा पोटाशियम, (iii) सोना और चांदी (iv) लेड तथा मरकरी।
7. मिश्रधातु क्या है ? तांबे के मिश्रधातु के दो उदाहरण दें।
उत्तर⇒ किसी धातु में अन्य धातु या अधातु की एक निश्चित मात्रा मिलाकर इच्छित गुण-धर्म वाली मिश्रधातुएँ प्राप्त की जा सकती हैं। ताम्बे के दो मिश्रधातु निम्नांकित हैं—पीतल और काँसा। पीतल में 80% Cu और काँसा में 90% Cu पाया
जाता है।
8. धातुएँ विद्युत के सुचालक क्यों होती हैं ?
उत्तर⇒ धातुएँ विद्युत के अच्छे चालक होते हैं। ये विद्युत धनात्मक भी हैं। इसमें इलेक्ट्रॉन त्यागने की प्रवृत्ति तीव्र होती है। ये ताप और विद्युत के सुचालक होते हैं। इसके तार से होकर विद्युत का प्रवाह आसानी से की जा सकती है। धातुओं को चालकता उनमें उपस्थित मुक्त इलेक्ट्रॉन के कारण होती है। ये इलेक्ट्रॉन धातु से होकर आसानी से दौड़ सकत हैं। यही कारण है कि धातु विद्युत और ताप के अच्छे चालक हैं।
9. संयोजकता से आप क्या समझते हैं ?
उत्तर⇒ किसी भी तत्त्व को संयाजकता उसक परमाण के सबसे बाहरी काश में उपस्थित संयाजकता इलक्ट्रॉनों की संख्या से निर्धारित होती है। मान लिया कि एक तत्त्व Na है। इसका परमाणु संख्या: 11 है। इसका इलेक्ट्रॉनिक विन्यास 2,8,1 है। अत: परमाण के बाहरी काश में इलेक्ट्रॉन संख्या । है। अत: इसकी संयोजकता 1 होगी।
10. आघातवर्थ्य तथा तन्य का अर्थ बताइए।
उत्तर⇒ कुछ धातुओं को पीटकर उनके चद्दर बनाए जाते हैं। इस गुणधर्म का आघातवर्थ्यता कहते हैं और धातु आघातवर्ध्य कहलाती है। किसी धातु के पतले तार खींचे जा सकते हैं। धातुओं के इस गुणधर्म को तन्यता कहते हैं तथा धातु तन्य कहलाती है। एक ग्राम सोने से 2 किमी लंबा तार बनाया जा सकता है।
11. संक्षारण से क्या समझते हैं?
उत्तर⇒ जब धात सतह जल, वायु अथवा आस-पास के अन्य किसा पदार्थ से प्रभावित होती है, तो इसे धातु का संक्षारित होना कहते हैं तथा इस परिघटना का संक्षारण कहा जाता है। गोल्ड तथा सिल्वर जैसी उत्कष्ट धातएँ सुगमतापूर्वक संक्षारित नहीं होती हैं। एलुमिनियम जैसी धातुएँ संक्षारित नहीं होती हैं।
12. संक्षारण से बचने की तीन विधियों को लिखें।
उत्तर⇒ संक्षारण रोकने की तीन विधियाँ –
(i) यशदलेपन द्वारा
(ii) विद्युत लेपन द्वारा
(iii) एनोडीकरण द्वारा
13. एक धातु और एक अधातु का नाम लिखें जो वायु के सम्पर्क में आने पर जल उठते हैं ?
उत्तर⇒ सोडियम धातु वायु के सम्पर्क में आन पर वायमंडलीय सामान्य ताप पर ही जल उठते हैं। श्वेत फॉस्फोरस अधातु है इसे पानी में डुबाकर रखा जाता है। यह वायु के सम्पर्क में आते ही जल उठता है।
14. जब धातुएँ नाइट्रिक अम्ल से अभिक्रिया करती है तो हाइड्रोजन गैस उत्सर्जित नहीं होता है। क्यों ?
उत्तर⇒ क्योंकि HNO3 एक प्रबल ऑक्सीकारक है जो उत्पन्न हाइड्रोजन का ऑक्सीकृत करके जल में परिवर्तित कर देता है एवं स्वयं नाइट्रोजन के किसी ऑक्साइड (N2O, NO, NO2 ) में अपचयित हो जाता है। लेकिन Mn ही एक ऐसा धातु है जो अति तनु HNO3 के साथ अभिक्रिया कर H2 गैस उत्पन्न करता है।
15. एनोड पंक क्या है? उदाहरण के साथ समझावें।
उत्तर⇒ विद्युत शोधन में जब विद्युत धारा प्रवाहित की जाती है तब एनोड पर स्थित अशद्ध धातु केटायन के रूप में घोल में जाने लगती है। उतनी ही मात्रा में शुद्ध धातु कैथोड पर जमा होती है। घुलनशील अशुद्धियाँ घोल में चली जाती हैं। अघुलनशील अशुद्धियाँ एनोड के नीचे जमा हो जाती हैं। इन्हें एनोड पंक कहते हैं।
16. निम्न पदों की परिभाषा दें–
(i) खनिज
(ii) अयस्क
(iii) गैंग
(iv) निस्तापन
(v) भर्जन
उत्तर⇒
(i) खनिज- भू-पर्पटी में प्राकृतिक रूप से पाए जाने वाले तत्त्वों या यौगिकों को खनिज कहते हैं। ये प्रायः खानों से निकाले जाते हैं।
(ii) अयस्क- वैसे खनिज जिनसे धातु का व्यावसायिक उत्पादन होता है, अयस्क कहलाते हैं। अयस्कों में धातु प्रचुर मात्रा में उपस्थित होते हैं। इससे धात का उत्पादन सरलता से कम खर्च में होता है।
(iii) गैंग- पथ्वी से प्राप्त खनिज अयस्कों में मिट्टी, रेत आदि कई अशद्धियाँ होती हैं। धातओं के निष्कर्षण स पहल अयस्क से अशुद्धियों को हटाना आवश्यक होता है। ये अशुद्धियाँ गैंग कहे जाते हैं। अयस्कों को गैंग से हटाने के लिए जिन प्रक्रियाओं का उपयोग होता है वे अयस्क एवं गैंग के भौतिक अथवा रासायनिक गुण धर्मों पर आधारित होते हैं। इनके पृथक्करण के लिए विभिन्न तकनीकों का उपयोग किया जाता है।
(iv) निस्तापन- अयस्क को उसके द्रवणांक से कम तापक्रम पर तीव्रता से गर्म करने की क्रिया जिससे उड़नशील अशुद्धियाँ बाहर निकल जाती हैं और ऑक्सीलवण ऑक्साइड में परिणत हो जाता है निस्तापन कहा जाता है। .
(v) भर्जन-अयस्क को वायु की अनियंत्रित आपूर्ति में उसके द्रवणांक से कम तापक्रम पर तीव्रता से गर्म करने की क्रिया भर्जन कहलाती है। इसमें अशुद्धियाँ ऑक्सीकृत होकर बाहर निकल जाती है।
17. आघातवर्ध्यता से क्या समझते हैं ?
उत्तर⇒ कुछ धातुओं को पीटकर चद्दर बनाए जाते हैं। इस गुणधर्म का आघातवर्ध्यता कहते हैं। इसी गुण के कारण एलुमिनियम के चद्दर, लोहे के चद्दर आदि बनाए जाते हैं।
18. पोटैशियम तथा सोडियम धातुओं को किरोसीन तेल में डुबाकर क्यों रखा जाता है?
उत्तर⇒ सोडियम तथा पोटैशियम तीव्र अभिक्रियाशील तत्त्व हैं। यह वायुमंडलीय ताप पर ही जल उठता है। अत: इसे खुले वायु में रखने से दुर्घटना की सम्भावना होती है। यही कारण है कि इसे किरोसीन तेल में डुबा कर रखा जाता है जिससे इसकी अभिक्रियाशीलता बिलकुल कम हो जाती है और यह वायमंडलीय ताप से अप्रभावित रहता है।
19.आयनिक यौगिकों के गलनांक उच्च क्यों होते हैं ?
उत्तर⇒ आयनिक यौगिक ठोस अवस्था में पाए जाते हैं। इनमें अंतर आण्विक आकर्षण बल काफी मजबूत होते हैं। अतः अंतर आण्विक आकर्षण को तोड़ने के लिए अधिक ऊर्जा की आवश्यकता होती है। यही कारण है कि आयनिक यौगिकों के गलनांक काफी उच्च होते हैं।
20. द्विधर्मी ऑक्साइड क्या है? उदाहरण दें।
उत्तर⇒ वैसे ऑक्साइड को द्विधर्मी अथवा उभयधर्मी ऑक्साइड कहे जाते हैं जिनमें अम्लीय और क्षारीय दानों गुण मौजूद होते हैं। जैसे एलुमिनियम ऑक्साइड। ये अम्लों और क्षारों से अभिक्रिया कर भिन्न-भिन्न यौगिकों का निर्माण करता है।
Al2O3 + 6HCI → 2AICI3 + 3H2O
Al2O3 + 2NaOH → 2NaAIO2 + H2O
21. कैरेट सोना का क्या अर्थ है ?
उत्तर⇒ शुद्ध सोने को 24 कैरेट कहते हैं। यह काफी नर्म होता है। इससे आभूषण बनाना कठिन है। आजकल गहने बनाने के लिए 22 कैरेट सोने की आवश्यकता होती है। 22 कैरेट सोना थोड़ा कठोर होता है। इसमें 22 भाग शुद्ध सोना और 2 भाग ताँबा या चाँदी मिला रहता है।
22. चाँदी, सोना एवं प्लैटिनम का उपयोग आभूषण बनाने में किया जाता है। क्यों ?
उत्तर⇒ सोना एक कोमल, सुनहले रंग का कीमती धातु है। इसका मुख्य उपयोग आभूषण बनाने में होता है। सोने की शुद्धता को कैरेट (Carat) में मापते हैं। शुद्ध सोना 24 कैरेट का होता है। आभूषण बनाते समय शुद्ध सोने में कम कीमती धात् ताँबा या चाँदी थोडा मिला दिया जाता है, जिससे वह कुछ कठोर बन जाता है। सोने के बने आभूषण 22 कैरेट के होते हैं। इसका अर्थ यह हुआ कि इन आभूषणों में 22 भाग सोना 2 भाग ताँबा या चाँदी की मिलावट है। 24 कैरेट सोना को 18 कैरेट सोना में बदलने के लिए 18 भाग सोना में 6 भाग ताँबा या चाँदी मिश्रित कर देते हैं। इस प्रकार चाँदी तथा प्लैटिनम का उपयोग किया जाता है
23. ध्वानिक (सोनोरस) किसे कहते हैं ?
उत्तर⇒ जब धातुएँ किसी कठोर सतह से टकराती है तो उनसे एक विशेष प्रकार की ध्वनि उत्पन्न होती है। इसे धातुई ध्वनि कहते हैं। इस प्रकार की धातुएँ ध्वानिक कहलाती हैं। स्कूल की घंटी से निकलने वाली ध्वनि इसका उदाहरण है।
24. एक्वारेजिया से क्या समझते हैं? इसके क्या उपयोग हैं ?
उत्तर⇒ एक्वारेजिया 3 : 1 के अनुपात में सांद्र हाइड्रोक्लोरिक अम्ल एवं सांद्र नाइट्रिक अम्ल का ताजा मिश्रण होता है। यह गोल्ड को गला सकता है। जबकि दोनों अम्लों में से प्रत्येक की यह क्षमता नहीं है। एक्वारेजिया भभकता द्रव होने के साथ प्रबल संक्षारक है। यह उन अभिकर्मकों में से एक है जो गोल्ड तथा प्लैटिनम को भी आसानी से गला सकता है।
25. थर्मिट अभिक्रिया क्या है?
उत्तर⇒ आयरन (III) ऑवसाइड ( Fe2O3 ) के साथ एल्युमीनियम की अभिक्रिया काफी तीव्र होती है और काफी ऊष्मा निकलता है इसका उपयोग रेल की पटरियों को जोड़ने में होता है। इस अभिक्रिया को थर्मिट अभिक्रिया कहते हैं।
26. अयस्कों के समृद्धीकरण से क्या तात्पर्य है ?
उत्तर⇒ पृथ्वी से निकलने वाले अयस्कों में मिट्टी, रेत आदि जैसी कई अशुद्धिया हटाना अयस्कों का समृद्धीकरण कहा जाता है।
27. लोहे को जंग से बचाने के दो उपाय बताइए।
उत्तर⇒ लोहे पर जंग लगने से बचाने के लिए लोहे की वस्तुओं पर पेंट करके, तेल लगाकर, ग्रीज लगाकर, यशद लेपन, क्रोमियम लेपन, एनोडीकरण या मिश्रधातु बनाकर आदि उपाय किए जाते हैं। इससे लोहे का संक्षारण रूक जाता है और लाह की वस्तुएँ बर्बाद होने से बच जाती है।
28. कॉपर को वायु में खुला छोड़ने पर वह हरे रंग का हो जाता है। क्यों ?
उत्तर⇒ कॉपर वायु में उपस्थित आर्द्र कार्बन डाइऑक्साइड के साथ अभिक्रिया करता है। जिससे इसकी सतह से भूरे रंग की चमक धीरे-धीरे खत्म हो जाती है तथा इस पर हरे रंग की चमक चढ़ जाती है। यह हरा पदार्थ कॉपर कार्बोनेट होता है।
29. हवाई जहाजों का ढाँचा ऐलुमिनियम के मिश्र धातुओं से क्यों बनाया जाता है ? वर्णन करें।
उत्तर⇒ हवाई जहाज का ढाँचा ऐलुमिनियम के मिश्र धातुओं डुरेलिमिन और मैग्लिनियम से निम्नलिखित कारणों से बनाया जाता है –
(i) ये अति हल्की मिश्र धातु है जिसका आपेक्षिक घनत्व बहुत कम है।
(ii) सुचालक होने के कारण विद्युत् प्रेषण तारें इनसे बनाई जा सकती हैं।
(iii) इन पर जंग नहीं लगता।
(iv) इन मिश्र धातुओं की कठोरता बहुत अधिक होती है।
(v) ये रसायनों के प्रति बहुत क्रियाशील नहीं है।
30. सल्फाइड अयस्क के सांद्रण के लिए फेन-उत्प्लावन विधि का संक्षेप में वर्णन करें।
उत्तर⇒ सल्फाइड अयस्कों का सांद्रण करने के लिए उन्हें खूब महीन पीसकर पाइन के तेल मिले जल के साथ मिलाकर हवा के झोके के द्वारा झाग पैदा किया जाता है। शुद्ध अयस्क झाग के साथ ऊपर आ जाता है तथा अशुद्धियाँ नीचे बैट जाती हैं। यह विधि फेन उत्प्लावन विधि कहलाती है।
31. सोडियम को केरोसीन तेल में डुबोकर क्यों रखा जाता है?
उत्तर⇒ सोडियम सक्रिय धातु है जो वायु में उपस्थित ऑक्सीजन से क्रिया करके सोडियम ऑक्साइड बनाती है। यह पानी से क्रिया कर सोडियम हाइड्रोक्साइड तथा हाइड्रोजन उत्पन्न करती है। वायु में खुला छोड़ देने पर यह आग पकड़ लेती है। इसलिए इसे मिट्टी के तेल में डुबोकर सुरक्षित रखते हैं।
32. वल्कनीकरण किसे कहते हैं ? इस प्रक्रिया में रबड़ में क्या परिवर्तन आते हैं ?
उत्तर⇒ सल्फर को प्राकृतिक रबड़ के साथ मिश्रित करने की प्रक्रिया को वल्कनीकरण कहते हैं। जब प्राकृतिक रबड़ को सल्फर से मिलाकर गर्म करते हैं तो रबड़ अधिक कठोर तथा कम लचकदार हो जाता है। रबड़ एक बहुलक है जिसमें एक ही तल में अणुओं की एक लंबी श्रृंखला होती है जिसके कारण रबड़ को खींचा जा सकता है परंतु सल्फर मिलाने से उसका लचीलापन समाप्त हो जाता है क्योंकि सल्फर रबड़ की श्रृंखला के समान अणुओं के मध्य आड़े बंध बनाता है। सल्फर कार्बन परमाणुओं के घूर्णन में भी बाधा डालती है।
33. खनिज और अयस्क क्या हैं ? लोहे के दो अयस्कों के नाम उनके आणविक सूत्र के साथ लिखें ।
उत्तर⇒ खनिज : ऐसे प्राकृतिक पदार्थ जिनमें धातुएँ अपने यौगिकों के रूप में होती हैं, खनिज कहलाते हैं। जैसे-फैल्सपार, अभ्रक आदि।
अयस्क : इन खनिजों को जिनसे लाभप्रद ढंग से धातुओं का निष्कर्षण किया जाता है, अयस्क कहलाते हैं। जैसे-हेमेटाइट, बॉक्साइट आदि।
लोहे के दो मुख्य अयस्क के नाम एक आण्विक सूत्र निम्नलिखित है-
(i) हेमाटाइट Fe2O3 एवं
(ii) आयरन पाइराइट FeS2
34. विद्यत अपघटनी शोधन से आप क्या समझते हैं ?
उत्तर⇒ कॉपर, जिंक, टिन, निकेल, चाँदी, सोना आदि जैसे अनेक धातुओं का शोधन विद्युत् अपघटन द्वारा किया जाता है । इस प्रक्रिया में अशुद्ध धातु को ऐनोड तथा शुद्ध धातु की पतली परत को कैथोड बनाया जाता है । धातु के लवण विलयन का उपयोग विद्युत्-अपघट्य के रूप में होता है। विद्युत-अपघट्य में जब धारा प्रवाहित होती है तब एनोड पर स्थित शुद्ध धातु विद्युत्-अपघट्य में घुल जाता है । इतनी ही मात्रा में शद्ध धात विद्यत-अपघटय से कैथोड पर निक्षेपित हो जाता है। विलयशील अशुद्धियाँ विलयन में चली जाती हैं तथा अविलयशील अशुद्धियाँ ऐनोड के नीचे निक्षेपित हो जाती हैं जिसे ऐनोड अवपंक कहते हैं।
35. Alloys स्टील क्या है ? किन्हीं तीन Alloy स्टील के नाम और उनकी संरचना लिखें।
उत्तर⇒ लोहे के साथ अन्य धातुओं और अधातुओं को मिलाकर प्राप्त की जाने वाली मिश्रधात स्टील कहलाती है।
इसके तीन प्रकार हैं-
(i) कार्बन स्टील- लोहे और कार्बन का मिश्र धातु कार्बन स्टील कहलाता है जिसमें कार्बन की मात्रा 0.5% से 1.5% तक होती है। कार्बन के अतिरिक्त सिलिकॉन, गन्धक, फॉस्फोरस तथा मैंगनीज भी होती है। कार्बन स्टील पेच, कील, गाड़ी की पटरियाँ, गार्डर तथा मशीनें बनाने में काम आता है । समुद्री जहाज, इमारतें तथा वाहन भी इसी से बनते हैं।
(ii) स्टेनलेस स्टील- जिसमें क्रोमियम, निकल, ताँबा, टंगस्टन या वेनडेनियम को मिलाया जाता है उसे स्टेनलेस स्टील कहते हैं। इसमें क्रोमियम 18% तथा निकल 8% होता है । यह डेयरी उद्योग अस्पतालों तथा बर्तन तैयार करने में काम आता है।
36. धातुकर्म क्या है ? इसके विभिन्न चरणों को लिखें।
उत्तर⇒ धातुकर्म वह विधि है जिसके द्वारा अयस्क से शुद्ध धातु का निष्कर्षण होता है।
अयस्क से शुद्ध धातु का निष्कर्षण कई चरणों में होता है –
(a) अयस्कों का समद्धीकरण- अयस्कों से गैंग को हटाने की प्रक्रिया को समृद्धीकरण कहते हैं।
(b) धातुओं का निष्कर्षण- इसके लिए निस्तापन, भर्जन, अपघटन आदि विधि का प्रयोग होता है।
(c) धातुओं का परिष्करण- अशुद्ध धातुओं को विभिन्न विधियों, जैसे विद्युत अपघटनी परिष्करण द्वारा शुद्ध किया जाता है।
37. एक मिश्रधातु क्या है ? मैग्नेलियम नामक मिश्रधातु के अवयवों के नाम लिखिए। इसके कोई दो उपयोग दीजिए।
उत्तर⇒ यह दो या दो से अधिक धातुओं अथवा तथा अधातु का संभागी मिश्रण है। उदाहरण—पीतल, तांबा तथा जिंक की मिश्रधातु है, कांसा, ताँबा तथा टिन की मिश्रधातु है।
मैग्नेलियम का संघटन-
ऐलुमिनियम (AI)-95%
मैग्नीशियम (Mg)-5%
मैग्नेलियम के उपयोग-
(i) हल्की तथा कठोर होने के कारण यह हवाई जहाज के भाग बनाने में प्रयोग की जाती है।
(ii) यह वाहनों तथा तुलाओं के भाग बनाने में काम आती है।
38. ऐलुमिनियम के उपयोग बताएँ।
उत्तर⇒ ऐलुमिनियम के उपयोग-
(i) ऐलुमिनियम हल्की धातु होने के कारण, हवाई जहाजों की बॉडी और मोटर इंजन बनाने के काम आती है।
(ii) यह बर्तन, फोटोफ्रेम तथा घरेलू उपयोग की ओर अनेक वस्तुएँ बनाने में काम आती है।
(iii) यह बिजली का सुचालक है, इसलिए आजकल बिजली के स्थानांतरण के लिए इनका प्रयोग किया जाता है।
(iv) ऐलमिनियम की बारीक परतों को खाने का सामान, दवाइयाँ दूध की बोतलें आदि पैक करने में प्रयुक्त की जाती हैं।
(v) ऐलुमिनियम पाउडर सिल्वर पेंट बनाने के काम आता है।
(vi) ऐलुमिनियम पाउडर एलूमिनोथिरैपी में प्रयुक्त होता है। यह प्रक्रम लोहे की पटरियों तथा मशीनों के टूटे भागों को जोड़ने के काम आता है।
39. अयस्क और खनिज में अंतर लिखिए।
उत्तर⇒ खनिज-धातुओं के प्राकृत यौगिक रूप को खनिज कहते हैं । अधिकांश धातुएँ हमें यौगिकों के रूप में ही प्राप्त होती हैं, जैसे-ताँबा हमें पाइराइट या क्यूपराइट से प्राप्त होता है। अयस्क-जिन पदार्थों (खनिजों) से धातु का निष्कर्षण सरल हो उन्हें अयस्क कहते हैं, जैसे- ऐलुमिनियम का अयस्क बॉक्साइट है तो लोहे का हैमेटाइट।
दोस्तों यहां पर क्लास 10th विज्ञान का धातु एवं अधातु चैप्टर का लघु उत्तरीय प्रश्न तथा दीर्घ उत्तरीय प्रश्न और साथ-साथ धातु एवं अधातु चैप्टर का ऑब्जेक्टिव क्वेश्चन का लिंक दिया गया है जहां से आप लोग इस चित्र का तैयारी अच्छे तरीके से कर सकते हैं। class 10th science Dhatu aur adhatu subjective Question
क्लास 10th विज्ञान बिहार बोर्ड प्रश्न उत्तर
1. कार्बनिक यौगिकों के कुछ गुणों को लिखें।
उत्तर⇒कार्बनिक यौगिकों के निम्नांकित गुण हैं-
(i) अधिकांश कार्बनिक यौगिक अच्छे विद्युत के चालक नहीं होते हैं।
(ii) इनके गलनांक एवं क्वथनांक निम्न होते हैं।
(iii) इनके परमाणुओं के बीच प्रबल आकर्षण बल नहीं होते हैं।
(iv) इन यौगिकों के आबंध से आयन की उत्पत्ति नहीं होती है।
(v) ये जल में घुलनशील नहीं होते हैं लेकिन पेट्रोल, डीजल, कार्बन डाइसल्फाइड जैसे-कार्बनिक पदार्थों में घुलनशील होते हैं।
| Also Read : class 10th science objective |
2. कार्बनिक यौगिकों की संख्या इतनी अधिक क्यों है ?
उत्तर⇒क्योंकि कार्बन परमाणु अन्य परमाणुओं के साथ इलेक्ट्रॉनों को साझा कर यौगिक बनाते हैं। यही कारण है कि कार्बनिक यौगिकों की संख्या इतनी अधिक है।
3. कार्बन के चार यौगिकों के नाम लिखें।
उत्तर⇒ एसिटीक एसिड – CH3COOH
क्लोरोफॉर्म – CH2Cl3
एथेनॉल – CH3CH2OH
मिथेन – CH4
4. कार्बन यौगिकों के तीन रासायनिक गुणधर्मों का उपयुक्त रासायनिक अभिक्रिया के साथ उल्लेख करें।
उत्तर⇒ (i) कार्बन यौगिक ऑक्सीकरण अभिक्रिया के फलस्वरूप ऊष्मा एवं प्रकाश उत्पन्न करते हैं।
CH4 + 02 → CO2+ H2O + ऊष्मा + प्रकाश
CH3CH2OH + 02 → CO2 + H2O + ऊष्मा + प्रकाश
(ii) एथनॉइक अम्ल क्षार (NaOH) के साथ अभिक्रिया कर सोडियम एसीटेट का निर्माण करता है।
NaOH + CH3COOH → CH3COONa + H2O
(iii) कार्बन यौगिक एथनॉल सोडियम के साथ अभिक्रिया कर सोडियम एथॉक्साइड तथा हाइड्रोजन गैस मुक्त करता है।
2Na + 2CH3CH2OH → 2CH3CH2O-Na+ + H2
5. कार्बन के दो गण-धर्म कौन-से हैं जिनके कारण हमारे चारों ओर कार्बन यौगिकों की विशाल संख्या दिखाई देती है ?
उत्तर⇒कार्बन की चतु: संयोजकता तथा शृंखलन दो ऐसे विशिष्ट गण हैं जिनके चलते कार्बन यौगिकों की संख्या अधिक है।
6. कार्बन के कितने अपरूप हैं। इनमें से कौन अधिक कठोर और कौन मुलायम है ?
उत्तर⇒कार्बन के मुख्यतः दो अपरूप हैं हीरा और ग्रेफाइट। हीरा काफी कठोर और ग्रेफाइट मुलायम होता है। हीरे का उपयोग गहना बनाने में और ग्रेफाइट का उपयोग लुब्रीकेंट के रूप में होता है।
7. कार्बनिक यौगिकों के क्वथनांक और गलनांक कम होते हैं, इससे इनकी प्रकृति के बारे में क्या कहा जा सकता है ?
उत्तर⇒कार्बनिक यौगिकों के क्वथनांक और गलनांक निम्न होने का कारण है कि इन यौगिकों के अणुओं के बीच प्रबल बंधन नहीं होते हैं। अतः बंधन बनाने के लिए आयनों का निर्माण नहीं करता है।
8. क्या आप डिटर्जेंट का उपयोग कर बता सकते हैं कि कोई जल कठोर है या नहीं ?
उत्तर⇒अपमार्जक (डिटर्जेंट) लंबी कार्बोक्सिलिक अम्ल श्रृंखला के अमोनियम एवं सल्फोनेट लवण होते हैं। इन यौगिकों का आवेशित सिरा कठोर जल में उपस्थित कैल्सियम एवं मैग्नीशियम आयनों के साथ अघुलनशील पदार्थ नहीं बनाते हैं। कठोर जल में भी अपमार्जक प्रभावी बने रहते हैं। ऐसी अवस्था में डिटर्जेंट का उपयोग कर कार्ड जल कठार है, इसके बारे में कहना कठिन है।
9. समजातीय श्रेणी किसे कहते हैं ?
उत्तर⇒कार्बन के यौगिकों का एक ऐसा समूह होता है जिसकी संरचनाएँ तथा रासायनिक गण समरूप होती हैं तथा दो क्रमागत सदस्यों के बीच CH.का अन्तर हाता हे समजातीय श्रेणी कहते हैं।
उदाहरण – एल्कन्स का समजातीय श्रेणी CH4 .C2H6 . C3H8 आदि है जिसके क्रमागत सदस्यों के बीच सदा -CH2 का अन्तर है।
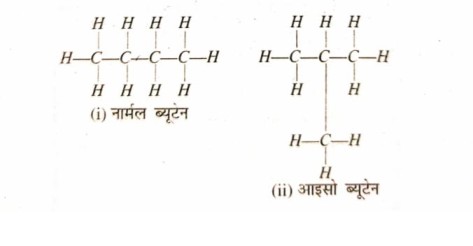
10. समावयवता किसे कहते हैं ? एक उदाहरण दें।
उत्तर⇒समान आण्विक सूत्र लेकिन विभिन्न संरचनाओं वाले ऐसे यौगिक संरचनात्मक समावयन कहलाते हैं। ये दो यौगिक ब्यूटेन के समावयवी कहे जाते हैं। ब्यूटन के दो समावयवी नॉर्मल ब्यूटेन और आइसो ब्यूटेन हैं। इस गुण को समावयवता कहते हैं।
ब्यूटेन का सूत्र C4H10 है।
11. एथनॉल के कुछ उपयोगों को लिखें।
उत्तर⇒ (i) इसका उपयोग टिंचर आयोडिन, कफ सीरप, टॉनिक आदि औषधियों के बनाने में होता है।
(ii) इसका उपयोग पीने में होता है।
(iii) शुद्ध एल्कोहल का उपयोग घातक है।
12. सह-संयोजी आबंध किसे कहते हैं ?
उत्तर⇒दो परमाणुओं के बीच इलेक्ट्रोन की एक युग्म की साझेदारी के द्वारा बनाने वाले आबंध सहसंयोजी आबंध कहलाते हैं। सह-संयोजी आबंध वाले अणुओं में भीतर तो प्रबल आबंध होता है लेकिन इनका अंतराणुक बल कम होता है। इन यौगिकों के क्वथनांक और गलनांक कम होते हैं। चूँकि परमाणुओं के बीच इलेक्ट्रोनों की साझेदारी होती है और आवेशित कण बनते हैं। ऐसे यौगिक विद्युत के कुचालक होते हैं।
13. डिटरजेंट कठोर जल में झाग क्यों देता है ?
उत्तर⇒का निर्माण कर साबुन के समान क्रिया करता है तथा झाग उत्पन्न करता है।
14. हाइड्रोजनीकरण क्या है? इसका औद्योगिक अनुप्रयोग क्या है ?
उत्तर⇒ वनस्पति तेलों में साधारणतः लंबी असंतृप्त कार्बन शृंखलाएँ होती हैं। निकेल उत्प्रेरक का उपयोग करके वनस्पति तेलों को हाइड्रोजनीकरण किया जाता है।

असंतृप्त हाइड्रोकार्बन को H से योग कर संतृप्त हाइड्रोकार्बन प्राप्त करना हाइड्रोजनीकरण कहलाता है।
15. समावयवी क्या है ?
उत्तर⇒ कुछ ऐसे कार्बनिक यौगिक होते हैं जिनके अणुसूत्र तो समान होते हैं लेकिन उनके संरचना सूत्र भिन्न-भिन्न होते हैं। ये यौगिक एक दूसरे के समावयवी कहे जाते हैं। यह गुण समावयवता कहलाती है। जैसे एथिल एल्कोहल और डायमिथायल ईथर। इनके अणु सूत्र C2H60 है।
16. हीरा और ग्रेफाइट के गुणों में अन्तर होने के क्या कारण हैं ?
उत्तर⇒ हीरा में प्रत्येक कार्बन परमाणु चार अन्य परमाणुओं से जुड़ा होता है। इस प्रकार एक दृढ़ त्रिआयामी संरचना बनती है। अतः हीरा अत्यन्त कठोर होता है।ग्रेफाइट में कार्बन परमाणु अन्य तीन कार्बन परमाणुओं से जुड़ा होता है। अतः यह हेक्सागोनल प्लेटों के रूप में रवा बनाता है। प्लेटों के बीच इलेक्ट्रॉन भरे रहने के कारण यह सुचालक भी है।
17. सिरका क्या है ? इसके उपयोगों को लिखें।
उत्तर⇒सिरका ऐथेनॉइक अम्ल का तनु घोल है। इसमें अन्य पदार्थ जैसे एस्टर, शर्करा, जेक्सट्रीन आदि तथा अन्य अम्ल घुले होते हैं। सिरके का उपयोग-सुगंध पैदा करने वाले पदार्थ और अचार आदि में परिरक्षक के रूप में भी किया जाता है।
18. एथनॉइक अम्ल के भौतिक गुण धर्मों को लिखें।
उत्तर⇒एथनॉइक अम्ल को साधारणतः एसिटीक अम्ल कहा जाता है। यह अम्ल कार्बोक्सिलिक अम्ल समूह से संबंधित है। एसिटीक अम्ल के 3-4% विलियन को सिरका कहा जाता है। यह अचार में परिरक्षक का काम करता है। शुद्ध एथनॉइक अम्ल का गलनांक 290 K होता है। शीत के मौसम में यह जम जाता है। इसलिए इसे ग्लैशियल एसिटीक अम्ल कहा जाता है। खनिज अम्लों की तुलना में इसकी अम्लीयता दुर्बल है। यह आयनीकृत नहीं होता है। यह जल में आसानी से घुल जाता है।
19.ईंधन के रूप में एल्कोहल का इस्तेमाल कैसे किया जाता है ?
उत्तर⇒गन्ना सूर्य के प्रकाश में रासायनिक ऊर्जा में बदलने में सर्वाधिक सक्षम होता है। गन्ने का रस (सिरका) बनाने के उपयोग में लाया जाता है जिसका किण्वन करके एल्कोहल तैयार किया जाता है। कुछ देशों में एल्कोहल में पेट्रोल मिलाकर स्वच्छ ईंधन के रूप में उपयोग किया जाता है। यह ईंधन पर्याप्त ऑक्सीजन होने पर केवल कार्बन डाइऑक्साइड एवं जल उत्पन्न करता है।
20. एथनॉल (C2H5OH) के भौतिक गुणधर्मों को लिखें।
उत्तर⇒एथनॉल के भौतिक गुणधर्म
(i) रंगहीन द्रव है।
(ii) इसका गंध सुनहला है।
(iii) यह उर्ध्वपतित द्रव है तथा इसका क्वथनांक 78°C (351 K) है।
(iv) यह जल से हल्का होता है।
(v) यह जल में घुलनशील है।
(vi) यह लिटमस के प्रति उदासीन है।
21. सजीव प्राणियों पर एल्कोहल का क्या प्रभाव पड़ता है ?
उत्तर⇒अधिक मात्रा में एथनॉल का सेवन करने पर उपापचयी प्रक्रिया धीमी पड़ जाती है। केन्द्रीय तंत्रिका तंत्र कमजोर हो जाता है। इसके कारण समन्वय की कमी हो जाती है, मानसिक दुविधा, अनिद्रा, भावशून्यता आ जाती है । मेथनॉल की थोड़ी-सी मात्रा लेने पर मृत्यु हो सकती है। मेथनॉल यकृत में ऑक्सीकृत होकर मेथेनैल बन जाता है। मेथेनैल यकृत की कोशिकाओं के घटकों के साथ शीघ्र अभिक्रिया करने लगता है। इससे प्रोटोप्लाज्म नष्ट होने लगता है। यह चक्षु तंत्रिका को भी प्रभावित करता है और व्यक्ति अंधा हो जाता है।
22. कठोर जल को साबुन से उपचारित करने पर मैली के निर्माण को समझाएँ।
उत्तर⇒ कैल्सियम तथा मैग्नीशियम लवणों की उपस्थिति के कारण जल कठोर हो जाता है। जब कठोर जल को साबुन से उपचारित किया जाता है तब साबुन कैल्सियम तथा मैग्नीशियम लवणों के साथ अभिक्रिया कर अविलय पदार्थ बनाते हैं। यह अविलेय पदार्थ मैली का निर्माण करते हैं।
23. जीवाश्म ईंधन से आप क्या समझते हैं ? इसका निर्माण कैसे होता है ?
उत्तर⇒करोड़ों वर्षों तक पृथ्वी की सतह में गहरे दबे हुए पौधों तथा पशुओं के अवशेषों से प्राप्त ईंधन को जीवाश्म ईंधन कहते हैं। कोयला और पेट्रोलियम जीवाश्म ईंधन हैं।
24. कार्बन तत्त्व एक अद्वितीय तत्त्व है। कैसे ?
उत्तर⇒ सभी ज्ञात परमाणुओं में से केवल कार्बन परमाणुओं में ही यह क्षमता कि वे आपस में मिलकर लंबी श्रृंखला बनाते हैं । प्रत्येक ऐसी लंबी श्रृंखला कार्बन परमाणु को इस प्रकार का सरल आधार प्रदान करती है जिसमें अन्य परमाण विभिन्न विधियों द्वारा जड सकते हैं जिसके परिणामस्वरूप कार्बन तत्त्व टाग किस्मों के यौगिक बनाए जा सकते हैं।
25. समजातीय श्रेणी क्या है ? उदाहरण के साथ समझाइए।
उत्तर⇒यौगिकों की ऐसी श्रृंखला जिसमें कार्बन श्रृंखला में स्थित हाइड्रोजन को एक ही प्रकार का प्रकार्यक समूह प्रतिस्थापित करता है उसे समजातीय श्रेणी कहते हैं। इसके दो क्रमागत सदस्यों में CH2 ग्रुप का अंतर होता है,
जैसे-एल्केन, सजातीय श्रेणी का सामान्य सूत्र CHnH2n+2है । इस श्रेणी के सदस्य मिथेन CH4 , इथेन C2H6, प्रोपेन C3H8 , ब्यूटेन C4H10 , पेंटेन C15 H12 , हैक्सेन C6H14 आदि हैं।
26. एस्टीरीफिकेशन (esterification) अभिक्रिया क्या है ? समीकरण द्वारा बतायें।
उत्तर⇒अम्ल तथा ऐल्कोहॉल की अभिक्रिया से ऐस्टर तथा जल बनते हैं। इस अभिक्रिया को ऐस्टरीकरण कहते है। उदाहरणार्थ ऐसीटिक अम्ल तथा ऐथिल ऐल्कोहॉल की अभिक्रिया से ऐस्टर ऐसीटेट का बनना ऐस्टरीकरण है।

27. सजातीय श्रेणी के लक्षण लिखें।
उत्तर⇒सजातीय श्रेणी के मख्य लक्षण निम्न हैं-
(i) किसी भी सजातीय श्रेणी के सभी सदस्यों को एक सामान्य सत्र के द्वारा प्रकट किया जा सकता है, जैसे एल्केन सजातीय श्रेणी के सभी सदस्योंएक ही सामान्य सूत्र CH, द्वारा प्रकट किया जाता है।
(ii) किसी भी सजातीय श्रेणी के दो साथ-साथ वाले सदस्यों में (_CH.) ग्रुप का अंतर होता है।
(iii) किसी भी सजातीय श्रेणी के सभी सदस्य एक जैसे रासायनिक गुण प्रकट करते हैं।
(iv) किसी भी सजातीय श्रेणी के सदस्यों के भौतिक गुणों में अणु भार बढ़ने के साथ-साथ क्रमिक परिवर्तन होता है।
(v) किसी भी सजातीय श्रेणी के सदस्यों को एक-सी विधियों द्वारा तैयार किया जा सकता है।
28. हाइड्रोकार्बन क्या है ? उदाहरण के साथ समझाइए।अथवा, विभिन्न प्रकार के हाइड्रोकार्बन के नाम उदाहरण सहित लिखिए।
उत्तर⇒ हाइड्रोजन और कार्बन से बने यौगिक को हाइड्रोकार्बन कहते हैं। हाइड्रोकार्बन दो प्रकार के होते हैं –
(i) संतप्त हाइडोकार्बन – सहसंयोजक एकल बंधनों से जुड़े कार्बन एवं हाइड्रोजन के यौगिक संतृप्त हाइड्रोकार्बन कहलाते हैं। इन्हें ऐल्केन भी कहा जाता है इनका सामान्य रासायनिक सूत्र (CnH2n+2) जैसे-मिथेन।
(ii) असंतप्त हाइड्रोकार्बन – खूली शृंखलावाले वे हाइड्रोकार्बन जिनमें कार्बन परमाणुओं के बीच द्विबंधन अथवा त्रिबंधन उपस्थित रहते हैं, असंतृप्त हाइड्रोकार्बन कहलाते हैं। कार्बन परमाणुओं के बीच द्विबंधन रहने पर हाइड्रोकार्बन को ऐल्कीन (alkene) कहते हैं। ऐल्कीन का सामान्य सूत्र CnH2n है। कार्बन परमाणुओं के बीच त्रिबंधन रहने पर हाइड्रोकार्बन को ऐल्काइन (alkyne) कहते हैं। ऐल्काइन. का सामान्य सूत्र (CnH2n-2 है।
29. मिथाइल ऐल्कोहल किस प्रकार तैयार किया जाता है ?
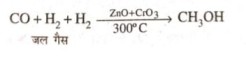
उत्तर⇒ मिथाइल ऐल्कोहल को वुड ऐल्कोहल या वुड स्प्रिट भी कहते हैं । इसे लकड़ी के भंजन से प्राप्त किया गया था। इसे तैयार करने के लिए लकड़ी के छोटे-छोटे टुकड़ों को वायु की अनुपस्थिति में गर्म किया जाता है। मिथाइल ऐल्कोहल एक उत्पाद के रूप में प्राप्त हो जाता है। आजकल इसे जल गैस तथा हाइड्रोजन के मिश्रण को 300°C तक गर्म करने से प्राप्त किया जाता है।
30. एस्टर किसे कहते हैं ? इन्हें किस प्रकार बनाया जाता है ? इनके दो उपयोग लिखिए।
उत्तर⇒जिन कार्बनिक यौगिकों का अभिलक्षकीय ग्रुप -C00- होता है, एस्टर कहलाते हैं। इनके निर्माण के लिए कार्बनिक अम्लों की सल्फ्यूरिक अम्ल की उपस्थिति में एल्कोहल से क्रिया कराई जाती है।

उपयोग – इनकी गंध फलों के समान होती है इसलिए इनका उपयोग ठंडे पेयों, आइसक्रीम, मिठाइयों तथा परफ्यूमों में होता है। ये फलों में भी पाए जाते हैं।
31. साबुनीकरण किसे कहते हैं ? प्रयोगशाला में साबुन किस प्रकार बनाते हैं ? वर्णन कीजिए।
उत्तर⇒जब वसा या तेल को NaOH के साथ गर्म किया जाता है तो वसा या तेल के अणु विघटित हो जाते हैं। इस प्रक्रिया को साबनीकरण कहते हैं जिसके फलस्वरूप साबुन बनता है।
प्रयोगशाला में साबुन की तैयारी —प्रयोगशाला में साबुन तैयार करने के लिए निम्नलिखित सामग्री चाहिए –
(i) वनस्पति तेल (जैसे, कैस्टर तेल, कॉटन सीड्ड तेल)
(ii) सोडियम हाइड्रोक्साइड (कास्टिक सोडा)
(iii) सोडियम क्लोराइड (साधारण नम)
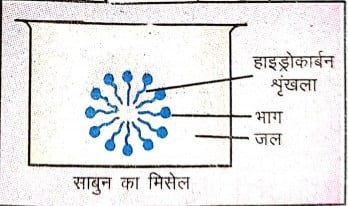
विधि – एक बीकर में 20 mL.कैस्टर ल लीजिए और उस 20%, 40 mLसोडियम हाइड्रोक्साइड का घोल डालिए। इस मिश्रण को धीरे-धीरे उबलने तक गर्म किया जाता है और इसेपाँच से दस मिनट तक उबालाजाता है। अब बीकर में 5 ग्राम खाने वाला नमक डालिए औरश्रृंखला पदार्थ को ठंडा होने दीजिए।ठंडा करने पर बीकर में साबुनजल बनता है जिसे तब हटा लिया जाता है ।
32. अपमार्जक किसे कहते हैं ? संश्लिष्ट अपमार्जक की संरचना बताइए। इसका प्रमुख लाभ लिखिए।
उत्तर⇒सफाई के लिए प्रयुक्त होने वाले पदार्थों को अपमार्जक कहते हैं। बहुत पहले से अपमार्जक के रूप में साबुन का प्रयोग होता रहा है परंतु आजकल संश्लिष्ट अपमार्जक अधिक लोकप्रिय हो गए हैं। संश्लिष्ट अपमार्जक में दो सिरों वाले अणु होते हैं जिनका एक सिरा जल को आकर्षित करता है जो प्रायः सल्फेट (-SO 4) या सल्फोनेट (-SO3Na) ग्रुप द्वारा बना होता है ।दूसरा सिरा जल को प्रतिकर्षित करता है जो हाइड्रोकार्बन युक्त होता है।
संश्लिष्ट अपमार्जक कठोर जल में भी पर्याप्त मात्रा में झाग बनाते हैं। ये कठोर जल के साथ अघुलनशील कैल्सियम या मैग्नेशियम के लवण नहीं बनाते हैं।
33. क्या कारण है कि ग्रेफाइट विद्युत् का सुचालक है ?
उत्तर⇒ ग्रेफाइट में प्रत्येक कार्बन परमाणु केवल तीन कार्बन परमाणुओं से सहसंयोजक बंधों द्वारा जुड़ा रहता है तथा जिस कारण इसमें षट्कोणीय जाल की परतें बनाते हैं। इसमें कार्बन परमाणुओं के बीच की दूरी अधिक होती है। परतों के मध्य इस दूरी के कारण विपरीत परतों में स्थित कार्बन परमाणुओं के बीच सहसंयोजक बंधों के बनने की संभावना समाप्त हो जाती है और चौथा संयोजक इलेक्ट्रॉन स्वतंत्र छूट जाता है। इसीलिए ग्रेफाइट में इलेक्ट्रॉनों का प्रवाह आसानी से हो जाता है और ग्रेफाइट विद्युत् का सुचालक हो जाता है।
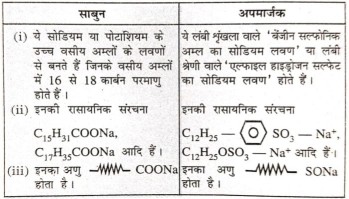
34. रासायनिक संरचना के आधार पर साबुन एवं अपमार्जक में विभेद कीजिए।
उत्तर⇒
1. कार्बनिक यौगिकों के कुछ गुणों को लिखें।
उत्तर⇒कार्बनिक यौगिकों के निम्नांकित गुण हैं-
(i) अधिकांश कार्बनिक यौगिक अच्छे विद्युत के चालक नहीं होते हैं।
(ii) इनके गलनांक एवं क्वथनांक निम्न होते हैं।
(iii) इनके परमाणुओं के बीच प्रबल आकर्षण बल नहीं होते हैं।
(iv) इन यौगिकों के आबंध से आयन की उत्पत्ति नहीं होती है।
(v) ये जल में घुलनशील नहीं होते हैं लेकिन पेट्रोल, डीजल, कार्बन डाइसल्फाइड जैसे-कार्बनिक पदार्थों में घुलनशील होते हैं।
| Also Read : class 10th science objective |
2. कार्बनिक यौगिकों की संख्या इतनी अधिक क्यों है ?
उत्तर⇒क्योंकि कार्बन परमाणु अन्य परमाणुओं के साथ इलेक्ट्रॉनों को साझा कर यौगिक बनाते हैं। यही कारण है कि कार्बनिक यौगिकों की संख्या इतनी अधिक है।
3. कार्बन के चार यौगिकों के नाम लिखें।
उत्तर⇒ एसिटीक एसिड – CH3COOH
क्लोरोफॉर्म – CH2Cl3
एथेनॉल – CH3CH2OH
मिथेन – CH4
4. कार्बन यौगिकों के तीन रासायनिक गुणधर्मों का उपयुक्त रासायनिक अभिक्रिया के साथ उल्लेख करें।
उत्तर⇒ (i) कार्बन यौगिक ऑक्सीकरण अभिक्रिया के फलस्वरूप ऊष्मा एवं प्रकाश उत्पन्न करते हैं।
CH4 + 02 → CO2+ H2O + ऊष्मा + प्रकाश
CH3CH2OH + 02 → CO2 + H2O + ऊष्मा + प्रकाश
(ii) एथनॉइक अम्ल क्षार (NaOH) के साथ अभिक्रिया कर सोडियम एसीटेट का निर्माण करता है।
NaOH + CH3COOH → CH3COONa + H2O
(iii) कार्बन यौगिक एथनॉल सोडियम के साथ अभिक्रिया कर सोडियम एथॉक्साइड तथा हाइड्रोजन गैस मुक्त करता है।
2Na + 2CH3CH2OH → 2CH3CH2O-Na+ + H2
5. कार्बन के दो गण-धर्म कौन-से हैं जिनके कारण हमारे चारों ओर कार्बन यौगिकों की विशाल संख्या दिखाई देती है ?
उत्तर⇒कार्बन की चतु: संयोजकता तथा शृंखलन दो ऐसे विशिष्ट गण हैं जिनके चलते कार्बन यौगिकों की संख्या अधिक है।
6. कार्बन के कितने अपरूप हैं। इनमें से कौन अधिक कठोर और कौन मुलायम है ?
उत्तर⇒कार्बन के मुख्यतः दो अपरूप हैं हीरा और ग्रेफाइट। हीरा काफी कठोर और ग्रेफाइट मुलायम होता है। हीरे का उपयोग गहना बनाने में और ग्रेफाइट का उपयोग लुब्रीकेंट के रूप में होता है।
7. कार्बनिक यौगिकों के क्वथनांक और गलनांक कम होते हैं, इससे इनकी प्रकृति के बारे में क्या कहा जा सकता है ?
उत्तर⇒कार्बनिक यौगिकों के क्वथनांक और गलनांक निम्न होने का कारण है कि इन यौगिकों के अणुओं के बीच प्रबल बंधन नहीं होते हैं। अतः बंधन बनाने के लिए आयनों का निर्माण नहीं करता है।
8. क्या आप डिटर्जेंट का उपयोग कर बता सकते हैं कि कोई जल कठोर है या नहीं ?
उत्तर⇒अपमार्जक (डिटर्जेंट) लंबी कार्बोक्सिलिक अम्ल श्रृंखला के अमोनियम एवं सल्फोनेट लवण होते हैं। इन यौगिकों का आवेशित सिरा कठोर जल में उपस्थित कैल्सियम एवं मैग्नीशियम आयनों के साथ अघुलनशील पदार्थ नहीं बनाते हैं। कठोर जल में भी अपमार्जक प्रभावी बने रहते हैं। ऐसी अवस्था में डिटर्जेंट का उपयोग कर कार्ड जल कठार है, इसके बारे में कहना कठिन है।
9. समजातीय श्रेणी किसे कहते हैं ?
उत्तर⇒कार्बन के यौगिकों का एक ऐसा समूह होता है जिसकी संरचनाएँ तथा रासायनिक गण समरूप होती हैं तथा दो क्रमागत सदस्यों के बीच CH.का अन्तर हाता हे समजातीय श्रेणी कहते हैं।
उदाहरण – एल्कन्स का समजातीय श्रेणी CH4 .C2H6 . C3H8 आदि है जिसके क्रमागत सदस्यों के बीच सदा -CH2 का अन्तर है।
10. समावयवता किसे कहते हैं ? एक उदाहरण दें।
उत्तर⇒समान आण्विक सूत्र लेकिन विभिन्न संरचनाओं वाले ऐसे यौगिक संरचनात्मक समावयन कहलाते हैं। ये दो यौगिक ब्यूटेन के समावयवी कहे जाते हैं। ब्यूटन के दो समावयवी नॉर्मल ब्यूटेन और आइसो ब्यूटेन हैं। इस गुण को समावयवता कहते हैं।
ब्यूटेन का सूत्र C4H10 है।

11. एथनॉल के कुछ उपयोगों को लिखें।
उत्तर⇒ (i) इसका उपयोग टिंचर आयोडिन, कफ सीरप, टॉनिक आदि औषधियों के बनाने में होता है।
(ii) इसका उपयोग पीने में होता है।
(iii) शुद्ध एल्कोहल का उपयोग घातक है।
12. सह-संयोजी आबंध किसे कहते हैं ?
उत्तर⇒दो परमाणुओं के बीच इलेक्ट्रोन की एक युग्म की साझेदारी के द्वारा बनाने वाले आबंध सहसंयोजी आबंध कहलाते हैं। सह-संयोजी आबंध वाले अणुओं में भीतर तो प्रबल आबंध होता है लेकिन इनका अंतराणुक बल कम होता है। इन यौगिकों के क्वथनांक और गलनांक कम होते हैं। चूँकि परमाणुओं के बीच इलेक्ट्रोनों की साझेदारी होती है और आवेशित कण बनते हैं। ऐसे यौगिक विद्युत के कुचालक होते हैं।
13. डिटरजेंट कठोर जल में झाग क्यों देता है ?
उत्तर⇒का निर्माण कर साबुन के समान क्रिया करता है तथा झाग उत्पन्न करता है।
14. हाइड्रोजनीकरण क्या है? इसका औद्योगिक अनुप्रयोग क्या है ?
उत्तर⇒ वनस्पति तेलों में साधारणतः लंबी असंतृप्त कार्बन शृंखलाएँ होती हैं। निकेल उत्प्रेरक का उपयोग करके वनस्पति तेलों को हाइड्रोजनीकरण किया जाता है।

असंतृप्त हाइड्रोकार्बन को H से योग कर संतृप्त हाइड्रोकार्बन प्राप्त करना हाइड्रोजनीकरण कहलाता है।
15. समावयवी क्या है ?
उत्तर⇒ कुछ ऐसे कार्बनिक यौगिक होते हैं जिनके अणुसूत्र तो समान होते हैं लेकिन उनके संरचना सूत्र भिन्न-भिन्न होते हैं। ये यौगिक एक दूसरे के समावयवी कहे जाते हैं। यह गुण समावयवता कहलाती है। जैसे एथिल एल्कोहल और डायमिथायल ईथर। इनके अणु सूत्र C2H60 है।
16. हीरा और ग्रेफाइट के गुणों में अन्तर होने के क्या कारण हैं ?
उत्तर⇒ हीरा में प्रत्येक कार्बन परमाणु चार अन्य परमाणुओं से जुड़ा होता है। इस प्रकार एक दृढ़ त्रिआयामी संरचना बनती है। अतः हीरा अत्यन्त कठोर होता है।ग्रेफाइट में कार्बन परमाणु अन्य तीन कार्बन परमाणुओं से जुड़ा होता है। अतः यह हेक्सागोनल प्लेटों के रूप में रवा बनाता है। प्लेटों के बीच इलेक्ट्रॉन भरे रहने के कारण यह सुचालक भी है।
17. सिरका क्या है ? इसके उपयोगों को लिखें।
उत्तर⇒सिरका ऐथेनॉइक अम्ल का तनु घोल है। इसमें अन्य पदार्थ जैसे एस्टर, शर्करा, जेक्सट्रीन आदि तथा अन्य अम्ल घुले होते हैं। सिरके का उपयोग-सुगंध पैदा करने वाले पदार्थ और अचार आदि में परिरक्षक के रूप में भी किया जाता है।
18. एथनॉइक अम्ल के भौतिक गुण धर्मों को लिखें।
उत्तर⇒एथनॉइक अम्ल को साधारणतः एसिटीक अम्ल कहा जाता है। यह अम्ल कार्बोक्सिलिक अम्ल समूह से संबंधित है। एसिटीक अम्ल के 3-4% विलियन को सिरका कहा जाता है। यह अचार में परिरक्षक का काम करता है। शुद्ध एथनॉइक अम्ल का गलनांक 290 K होता है। शीत के मौसम में यह जम जाता है। इसलिए इसे ग्लैशियल एसिटीक अम्ल कहा जाता है। खनिज अम्लों की तुलना में इसकी अम्लीयता दुर्बल है। यह आयनीकृत नहीं होता है। यह जल में आसानी से घुल जाता है।
19.ईंधन के रूप में एल्कोहल का इस्तेमाल कैसे किया जाता है ?
उत्तर⇒गन्ना सूर्य के प्रकाश में रासायनिक ऊर्जा में बदलने में सर्वाधिक सक्षम होता है। गन्ने का रस (सिरका) बनाने के उपयोग में लाया जाता है जिसका किण्वन करके एल्कोहल तैयार किया जाता है। कुछ देशों में एल्कोहल में पेट्रोल मिलाकर स्वच्छ ईंधन के रूप में उपयोग किया जाता है। यह ईंधन पर्याप्त ऑक्सीजन होने पर केवल कार्बन डाइऑक्साइड एवं जल उत्पन्न करता है।
20. एथनॉल (C2H5OH) के भौतिक गुणधर्मों को लिखें।
उत्तर⇒एथनॉल के भौतिक गुणधर्म
(i) रंगहीन द्रव है।
(ii) इसका गंध सुनहला है।
(iii) यह उर्ध्वपतित द्रव है तथा इसका क्वथनांक 78°C (351 K) है।
(iv) यह जल से हल्का होता है।
(v) यह जल में घुलनशील है।
(vi) यह लिटमस के प्रति उदासीन है।
21. सजीव प्राणियों पर एल्कोहल का क्या प्रभाव पड़ता है ?
उत्तर⇒अधिक मात्रा में एथनॉल का सेवन करने पर उपापचयी प्रक्रिया धीमी पड़ जाती है। केन्द्रीय तंत्रिका तंत्र कमजोर हो जाता है। इसके कारण समन्वय की कमी हो जाती है, मानसिक दुविधा, अनिद्रा, भावशून्यता आ जाती है । मेथनॉल की थोड़ी-सी मात्रा लेने पर मृत्यु हो सकती है। मेथनॉल यकृत में ऑक्सीकृत होकर मेथेनैल बन जाता है। मेथेनैल यकृत की कोशिकाओं के घटकों के साथ शीघ्र अभिक्रिया करने लगता है। इससे प्रोटोप्लाज्म नष्ट होने लगता है। यह चक्षु तंत्रिका को भी प्रभावित करता है और व्यक्ति अंधा हो जाता है।
22. कठोर जल को साबुन से उपचारित करने पर मैली के निर्माण को समझाएँ।
उत्तर⇒ कैल्सियम तथा मैग्नीशियम लवणों की उपस्थिति के कारण जल कठोर हो जाता है। जब कठोर जल को साबुन से उपचारित किया जाता है तब साबुन कैल्सियम तथा मैग्नीशियम लवणों के साथ अभिक्रिया कर अविलय पदार्थ बनाते हैं। यह अविलेय पदार्थ मैली का निर्माण करते हैं।
23. जीवाश्म ईंधन से आप क्या समझते हैं ? इसका निर्माण कैसे होता है ?
उत्तर⇒करोड़ों वर्षों तक पृथ्वी की सतह में गहरे दबे हुए पौधों तथा पशुओं के अवशेषों से प्राप्त ईंधन को जीवाश्म ईंधन कहते हैं। कोयला और पेट्रोलियम जीवाश्म ईंधन हैं।
24. कार्बन तत्त्व एक अद्वितीय तत्त्व है। कैसे ?
उत्तर⇒ सभी ज्ञात परमाणुओं में से केवल कार्बन परमाणुओं में ही यह क्षमता कि वे आपस में मिलकर लंबी श्रृंखला बनाते हैं । प्रत्येक ऐसी लंबी श्रृंखला कार्बन परमाणु को इस प्रकार का सरल आधार प्रदान करती है जिसमें अन्य परमाण विभिन्न विधियों द्वारा जड सकते हैं जिसके परिणामस्वरूप कार्बन तत्त्व टाग किस्मों के यौगिक बनाए जा सकते हैं।
25. समजातीय श्रेणी क्या है ? उदाहरण के साथ समझाइए।
उत्तर⇒यौगिकों की ऐसी श्रृंखला जिसमें कार्बन श्रृंखला में स्थित हाइड्रोजन को एक ही प्रकार का प्रकार्यक समूह प्रतिस्थापित करता है उसे समजातीय श्रेणी कहते हैं। इसके दो क्रमागत सदस्यों में CH2 ग्रुप का अंतर होता है,
जैसे-एल्केन, सजातीय श्रेणी का सामान्य सूत्र CHnH2n+2है । इस श्रेणी के सदस्य मिथेन CH4 , इथेन C2H6, प्रोपेन C3H8 , ब्यूटेन C4H10 , पेंटेन C15 H12 , हैक्सेन C6H14 आदि हैं।
26. एस्टीरीफिकेशन (esterification) अभिक्रिया क्या है ? समीकरण द्वारा बतायें।
उत्तर⇒अम्ल तथा ऐल्कोहॉल की अभिक्रिया से ऐस्टर तथा जल बनते हैं। इस अभिक्रिया को ऐस्टरीकरण कहते है। उदाहरणार्थ ऐसीटिक अम्ल तथा ऐथिल ऐल्कोहॉल की अभिक्रिया से ऐस्टर ऐसीटेट का बनना ऐस्टरीकरण है।

27. सजातीय श्रेणी के लक्षण लिखें।
उत्तर⇒सजातीय श्रेणी के मख्य लक्षण निम्न हैं-
(i) किसी भी सजातीय श्रेणी के सभी सदस्यों को एक सामान्य सत्र के द्वारा प्रकट किया जा सकता है, जैसे एल्केन सजातीय श्रेणी के सभी सदस्योंएक ही सामान्य सूत्र CH, द्वारा प्रकट किया जाता है।
(ii) किसी भी सजातीय श्रेणी के दो साथ-साथ वाले सदस्यों में (_CH.) ग्रुप का अंतर होता है।
(iii) किसी भी सजातीय श्रेणी के सभी सदस्य एक जैसे रासायनिक गुण प्रकट करते हैं।
(iv) किसी भी सजातीय श्रेणी के सदस्यों के भौतिक गुणों में अणु भार बढ़ने के साथ-साथ क्रमिक परिवर्तन होता है।
(v) किसी भी सजातीय श्रेणी के सदस्यों को एक-सी विधियों द्वारा तैयार किया जा सकता है।
28. हाइड्रोकार्बन क्या है ? उदाहरण के साथ समझाइए।अथवा, विभिन्न प्रकार के हाइड्रोकार्बन के नाम उदाहरण सहित लिखिए।
उत्तर⇒ हाइड्रोजन और कार्बन से बने यौगिक को हाइड्रोकार्बन कहते हैं। हाइड्रोकार्बन दो प्रकार के होते हैं –
(i) संतप्त हाइडोकार्बन – सहसंयोजक एकल बंधनों से जुड़े कार्बन एवं हाइड्रोजन के यौगिक संतृप्त हाइड्रोकार्बन कहलाते हैं। इन्हें ऐल्केन भी कहा जाता है इनका सामान्य रासायनिक सूत्र (CnH2n+2) जैसे-मिथेन।
(ii) असंतप्त हाइड्रोकार्बन – खूली शृंखलावाले वे हाइड्रोकार्बन जिनमें कार्बन परमाणुओं के बीच द्विबंधन अथवा त्रिबंधन उपस्थित रहते हैं, असंतृप्त हाइड्रोकार्बन कहलाते हैं। कार्बन परमाणुओं के बीच द्विबंधन रहने पर हाइड्रोकार्बन को ऐल्कीन (alkene) कहते हैं। ऐल्कीन का सामान्य सूत्र CnH2n है। कार्बन परमाणुओं के बीच त्रिबंधन रहने पर हाइड्रोकार्बन को ऐल्काइन (alkyne) कहते हैं। ऐल्काइन. का सामान्य सूत्र (CnH2n-2 है।
29. मिथाइल ऐल्कोहल किस प्रकार तैयार किया जाता है ?
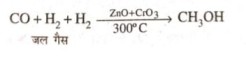
उत्तर⇒ मिथाइल ऐल्कोहल को वुड ऐल्कोहल या वुड स्प्रिट भी कहते हैं । इसे लकड़ी के भंजन से प्राप्त किया गया था। इसे तैयार करने के लिए लकड़ी के छोटे-छोटे टुकड़ों को वायु की अनुपस्थिति में गर्म किया जाता है। मिथाइल ऐल्कोहल एक उत्पाद के रूप में प्राप्त हो जाता है। आजकल इसे जल गैस तथा हाइड्रोजन के मिश्रण को 300°C तक गर्म करने से प्राप्त किया जाता है।
30. एस्टर किसे कहते हैं ? इन्हें किस प्रकार बनाया जाता है ? इनके दो उपयोग लिखिए।
उत्तर⇒जिन कार्बनिक यौगिकों का अभिलक्षकीय ग्रुप -C00- होता है, एस्टर कहलाते हैं। इनके निर्माण के लिए कार्बनिक अम्लों की सल्फ्यूरिक अम्ल की उपस्थिति में एल्कोहल से क्रिया कराई जाती है।

उपयोग – इनकी गंध फलों के समान होती है इसलिए इनका उपयोग ठंडे पेयों, आइसक्रीम, मिठाइयों तथा परफ्यूमों में होता है। ये फलों में भी पाए जाते हैं।
31. साबुनीकरण किसे कहते हैं ? प्रयोगशाला में साबुन किस प्रकार बनाते हैं ? वर्णन कीजिए।
उत्तर⇒जब वसा या तेल को NaOH के साथ गर्म किया जाता है तो वसा या तेल के अणु विघटित हो जाते हैं। इस प्रक्रिया को साबनीकरण कहते हैं जिसके फलस्वरूप साबुन बनता है।
प्रयोगशाला में साबुन की तैयारी —प्रयोगशाला में साबुन तैयार करने के लिए निम्नलिखित सामग्री चाहिए –
(i) वनस्पति तेल (जैसे, कैस्टर तेल, कॉटन सीड्ड तेल)
(ii) सोडियम हाइड्रोक्साइड (कास्टिक सोडा)
(iii) सोडियम क्लोराइड (साधारण नम)

विधि – एक बीकर में 20 mL.कैस्टर ल लीजिए और उस 20%, 40 mLसोडियम हाइड्रोक्साइड का घोल डालिए। इस मिश्रण को धीरे-धीरे उबलने तक गर्म किया जाता है और इसेपाँच से दस मिनट तक उबालाजाता है। अब बीकर में 5 ग्राम खाने वाला नमक डालिए औरश्रृंखला पदार्थ को ठंडा होने दीजिए।ठंडा करने पर बीकर में साबुनजल बनता है जिसे तब हटा लिया जाता है ।
32. अपमार्जक किसे कहते हैं ? संश्लिष्ट अपमार्जक की संरचना बताइए। इसका प्रमुख लाभ लिखिए।
उत्तर⇒सफाई के लिए प्रयुक्त होने वाले पदार्थों को अपमार्जक कहते हैं। बहुत पहले से अपमार्जक के रूप में साबुन का प्रयोग होता रहा है परंतु आजकल संश्लिष्ट अपमार्जक अधिक लोकप्रिय हो गए हैं। संश्लिष्ट अपमार्जक में दो सिरों वाले अणु होते हैं जिनका एक सिरा जल को आकर्षित करता है जो प्रायः सल्फेट (-SO 4) या सल्फोनेट (-SO3Na) ग्रुप द्वारा बना होता है ।दूसरा सिरा जल को प्रतिकर्षित करता है जो हाइड्रोकार्बन युक्त होता है।
संश्लिष्ट अपमार्जक कठोर जल में भी पर्याप्त मात्रा में झाग बनाते हैं। ये कठोर जल के साथ अघुलनशील कैल्सियम या मैग्नेशियम के लवण नहीं बनाते हैं।
33. क्या कारण है कि ग्रेफाइट विद्युत् का सुचालक है ?
उत्तर⇒ ग्रेफाइट में प्रत्येक कार्बन परमाणु केवल तीन कार्बन परमाणुओं से सहसंयोजक बंधों द्वारा जुड़ा रहता है तथा जिस कारण इसमें षट्कोणीय जाल की परतें बनाते हैं। इसमें कार्बन परमाणुओं के बीच की दूरी अधिक होती है। परतों के मध्य इस दूरी के कारण विपरीत परतों में स्थित कार्बन परमाणुओं के बीच सहसंयोजक बंधों के बनने की संभावना समाप्त हो जाती है और चौथा संयोजक इलेक्ट्रॉन स्वतंत्र छूट जाता है। इसीलिए ग्रेफाइट में इलेक्ट्रॉनों का प्रवाह आसानी से हो जाता है और ग्रेफाइट विद्युत् का सुचालक हो जाता है।
34. रासायनिक संरचना के आधार पर साबुन एवं अपमार्जक में विभेद कीजिए।
उत्तर⇒

